Un equipo de investigadores de la UPM, en colaboración con otras universidades, descubre la existencia de subtipos de pacientes y establece las pautas para un mejor tratamiento.
Investigadores del Centro de Tecnología Biomédica (CTB) de la Universidad Politécnica de Madrid (UPM) han participado en un estudio junto a la Universidad Carlos III de Madrid y la Universidad de Reading (Reino Unido) que ha desvelado la posible existencia de subtipos de pacientes de párkinson. A partir de este nuevo conocimiento, han aplicado técnicas de inteligencia artificial para la detección del temblor en pacientes de los grupos hallados. El objetivo es conseguir una estimulación cerebral bajo demanda que palie los síntomas de la enfermedad de una manera más inteligente, lo que en el futuro redundará en una mejor calidad de vida de los pacientes.
La enfermedad de Parkinson es una patología del sistema motor cuya sintomatología principal incluye temblor, rigidez y bradicinesia. La función motora es un equilibrio meticulosamente regulado por una serie de neurotransmisores en los circuitos de los ganglios basales. Cuando uno de los neurotransmisores no es liberado de forma correcta, la información entre núcleos no es eficiente y deriva en enfermedades del sistema motor. Este es el caso del párkinson, en el que la causa principal es la muerte de neuronas secretoras de dopamina. El trabajo de los investigadores del Grupo de Neurociencia Cognitiva y Computacional del CTB-UPM se ha centrado en el estudio del síntoma más conocido del párkinson, el temblor.
Existen diferentes tipos de temblor en la enfermedad de Parkinson dependiendo de las circunstancias en las que aparezca. El más común es el llamado temblor en reposo (RT), un movimiento rítmico que aparece cuando el paciente está en reposo y suele desaparecer cuando el paciente inicia un movimiento. Es un síntoma muy deshabilitante para el paciente, ya que le impide realizar de manera normal las actividades de la vida diaria.
Algunos estudios sugieren que el párkinson es en realidad una denominación que agrupa diferentes subtipos de esta enfermedad, ya que no todos los pacientes presentan la misma sintomatología ni responden de la misma manera al tratamiento.
El tratamiento de la enfermedad de Parkinson es a día de hoy una tarea compleja. La primera opción es la medicación oral, que consiste en el suministro de levodopa (principal precursor de la dopamina). Su uso comenzó a mediados de los años sesenta pero sigue siendo el tratamiento más utilizado. El tratamiento con levodopa alivia la principal sintomatología del párkinson, sin embargo no se adapta correctamente a la evolución de la enfermedad. Después de unos pocos años de uso se calcula que alrededor de cinco, los pacientes comienzan a experimentar fluctuaciones motoras. Este es el conocido efecto on-off, en el que se alternan los periodos en los que medicación hace afecto (on) con periodos en los que no (off). Además, los periodos off aumentan en duración a medida que aumenta el tiempo de uso del tratamiento, haciéndose la medicación oral cada vez más inadecuada.
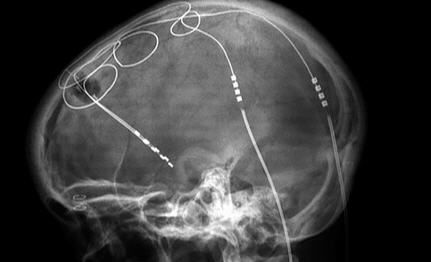
Debido a estas, entre otras, complicaciones con el tratamiento oral, algunos pacientes son sometidos a tratamiento quirúrgico para ser tratados con estimulación cerebral profunda. Esta terapia consiste en la implantación de electrodos que aplican una estimulación eléctrica justo en las estructuras cerebrales afectadas. En el caso del párkinson, normalmente se trata del núcleo subtalámico. Este estímulo rompe con la actividad anormal de las neuronas, que caen en una excesiva sincronización, imponiendo un ritmo de funcionamiento correcto.
Aunque los neuroestimuladores se conocen como los “marcapasos cerebrales”, no trabajan de la misma manera. Mientras los marcapasos son capaces de detectar episodios atípicos en la señal cardiaca y adaptar la estimulación a las necesidades del paciente en cada momento, los neuroestimuladores realizan, una vez implantados, una estimulación continuada. Esto supone, entre otras cosas, que la batería del dispositivo tenga que ser reemplazada cada 3 o 4 años, obligando al paciente a someterse a una nueva cirugía.
La contribución principal del nuevo estudio de investigación es haber hallado resultados que, con un alto grado de certeza, indican la existencia de dos subtipos de pacientes, o más específicamente de temblor de tipo 1, según la Declaración de Consenso de la Sociedad de Trastornos del Movimiento en Temblor. Tales resultados pueden conducir al desarrollo de diferentes tratamientos para los distintos tipos de pacientes involucrados.
Por otro lado, y partiendo del conocimiento hallado, el estudio propone un sistema de detección del temblor en tiempo real basado en redes de neuronas artificiales. Los investigadores proponen desarrollar una herramienta que aprenda diferentes características de la señal cerebral cuando el paciente tiembla. Entrenando esta máquina, esta sería capaz de decidir cuándo el paciente está sufriendo un episodio de temblor y cuándo no, siendo el entorno de trabajo un ordenador. La idea es que cuando un sistema de estimulación bajo demanda como el propuesto sea 100% fiable se empotre en el neuroestimulador.
Un sistema de estimulación bajo demanda sería capaz de detectar cuándo el paciente está temblando y solo entonces proporcionarle estimulación. Los beneficios de esto son dobles: por un lado, se permitiría a las estructuras cerebrales realizar su función de manera normal cuando el paciente no presente síntomas, en lugar de ser estimuladas todo el rato; y, por otro lado, el uso de la batería sería más eficiente, alargando su vida útil y, por tanto, el tiempo de uso antes de pasar por cirugía a sustituirla.
De esta forma, se puede dotar a los dispositivos médicos implantables de cierta inteligencia. Así, podrán aprender de la patología del paciente que los porta y tener capacidad de decisión para mejorar su tratamiento y, por ende, su vida diaria.
(Universidad Politécnica de Madrid)