Un grupo de jóvenes bioingenieros de varias nacionalidades, entre ellos el español Carlos Castro, ha desarrollado un dispositivo portátil capaz de contar glóbulos blancos en tiempo real, sin necesidad de una muestra de sangre. Se trata de un sensor óptico que, a través de la piel, detecta y cuantifica los leucocitos cuando fluyen bajo una lente diminuta. Las aplicaciones del sistema, que podría estar en el mercado en 2019, van desde mejorar el tratamiento de pacientes a los que la quimioterapia deja sin defensas a la prevención de sepsis.
El proyecto, denominado Leuko, ha logrado financiación de Madrid-MIT M+Visión, un consorcio que busca impulsar la colaboración entre centros de investigación y hospitales de la Comunidad de Madrid con el Instituto Tecnológico de Massachusetts (MIT) y otros centros del área de Boston (EE UU). También ha contado con aportaciones de dos instituciones estadounidenses: Center of Future Technologies in Cancer Care y Coulter Foundation. La cifra total conseguida para sacar adelante la idea ha sido de 400.000 euros.
Según explica a Sinc Carlos Castro, un ingeniero especializado en biomedicina que trabaja en el Research Laboratory of Electronics del MIT en Boston, “la tecnología permitirá facilitar la medición de glóbulos blancos de manera indolora y sencilla. Al igual que los diabéticos disponen de un glucómetro con el que controlan sus niveles de glucosa, los pacientes sometidos a quimioterapia podrán usar en un futuro un ‘leukometro’ para estimar el estado de sus defensas”.
Linfoma y leucemia
Con esto –agrega– se abre la posibilidad de personalizar la quimioterapia según la respuesta inmunológica de cada paciente. Especialmente en enfermos de linfoma o leucemia, “las dosis del tratamiento se podrían maximizar para cada individuo sin comprometer su sistema inmunológico. Así se podría mejorar la eficacia de la terapia al tiempo que se reduce la probabilidad de graves infecciones”.
Castro cuenta que la idea de desarrollar la tecnología surgió hace dos años durante una estancia clínica que el equipo realizó en el Hospital Gregorio Marañón de Madrid. Allí, los investigadores constataron que la inmunosupresión (bajos recuentos de glóbulos blancos) es el principal efecto secundario para pacientes de quimioterapia, lo cual desemboca en infecciones, hospitalizaciones, retrasos de dosis y peor esperanza de vida.
A partir de este momento “vimos la necesidad de crear un dispositivo no invasivo que permitiera detectar la leucopenia de forma temprana y así actuar para evitar sus consecuencias”, indica.
La tecnología utilizada incluye un sistema óptico portátil que proporciona iluminación oblicua con LED y es capaz de tomar imágenes de capilares superficiales bajo la piel a un nivel resolución celular, dice el experto. Los vídeos adquiridos son después automáticamente analizados por algoritmos capaces de detectar los glóbulos blancos y calcular su concentración. Estos algoritmos, que se han protegido ya mediante una patente, fueron presentados en una conferencia del Instituto de Ingeniería Eléctrica y Electrónica (IEEE), celebrada en Milán el pasado mes de agosto.
Modo de empleo
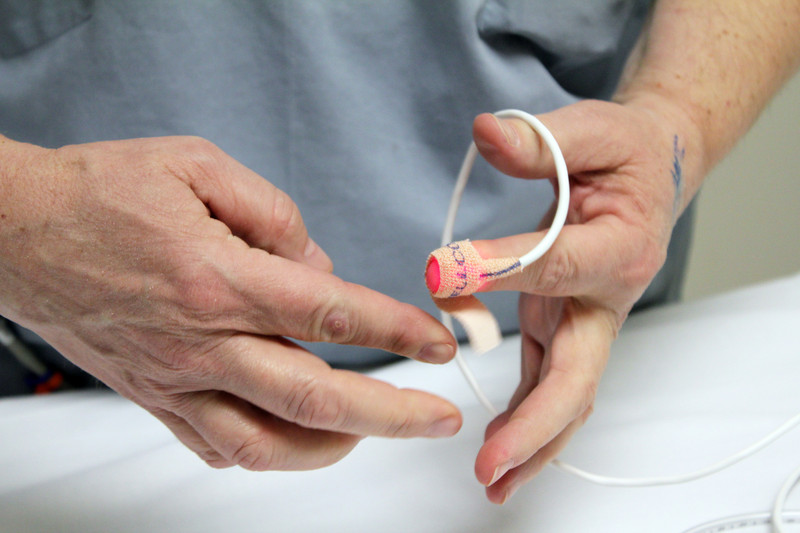
Castro explica que el dispositivo se coloca sobre el dedo del paciente, de manera similar a los pulsioxímetros que se usan en hospitales para medir los niveles de oxígeno en sangre. Mediante una pequeña lente, el sistema adquiere imágenes de capilares muy superficiales en el lecho ungeal, bajo la uña.
Al iluminar a determinadas frecuencias, la luz es absorbida por la hemogoblina en los glóbulos rojos, un efecto que no sucede en los glóbulos blancos. Esto hace que los leucocitos aparezcan como pequeñas partículas transparentes moviéndose dentro del capilar.
Después, “nuestros algoritmos de procesado de imagen reconocen dichos eventos y los cuentan proporcionando una estimación de su nivel en la sangre”, agrega el investigador.
En su opinión, la facilidad de uso y la portabilidad del dispositivo abren la posibilidad futura de que los pacientes puedan realizar estas mediciones desde su casa. Ya no será necesario desplazarse a un centro hospitalario o ambulatorio. “En zonas rurales con acceso limitado a centros sanitarios, o en países en vías de desarrollo, esto se convierte en una gran ventaja. Además, también sería posible realizar mediciones de manera más continua abriendo opciones de tratamiento que hasta ahora no eran posibles”, subraya.
Tratamientos más personalizados
Si, por ejemplo, se detecta que los glóbulos blancos de un paciente de quimioterapia están demasiado bajos, se podrían prescribir inmediatamente medicamentos que estimularan su producción evitando una posible infección. O si se observa que la persona se ha recuperado antes de tiempo, se le podría aplicar anticipadamente una nueva dosis en su tratamiento para mejorar su eficacia y reducir el tiempo de recuperación. “Estas decisiones no son posibles actualmente porque no es viable llamar a los pacientes cada hora o cada día para realizarles un análisis de sangre”, dice Castro.
El ingeniero añade que además de su aplicación en quimioterapia “existen otros ámbitos médicos en los que este dispositivo podría tener un gran impacto, desde su uso para prevenir sepsis a la diferenciación temprana entre infecciones bacterianas o víricas que constituyen una amenaza para 4.000 millones de personas en todo el mundo”.
En este momento, el equipo integrado por Castro, Ian Butterworth,Álvaro Sánchez, Aurélien Bourquard y Luis Soenksen, está llevado a cabo la prueba de concepto técnica y han establecido colaboraciones para probar los primeros prototipos clínicamente. Entre las instituciones con las que están trabajando figuran la Universidad de Boston, el Massachusetts General Hospital, el Hospital de Fuenlabrada (Madrid), la Universidad Politécnica de Madrid y el Centro Nacional de Investigaciones Oncológicas (CNIO).
Tres prototipos
Actualmente, están en desarrollo tres prototipos distintos. Uno de ellos es un microscopio portátil que se coloca manualmente sobre el dedo del paciente para tomar vídeos de su microcirculación en capilares muy superficiales. Este dispositivo ya se ha probado con 31 pacientes en el Hospital de Fuenlabrada y con seis más en el Massachusetts General Hospital. “Ahora, estamos trabajando para mejorar su precisión y fiabilidad”, señala Castro.
Una segunda versión del prototipo incluye modificaciones en el microscopio para mejorar la estabilidad y calidad de las imágenes. Y en el tercero, una pequeña pieza óptica puede colocarse en la cámara de un teléfono móvil para obtener imágenes de la circulación en los capilares. “Estas imágenes se podrían transmitir después a un servidor donde los algoritmos las analizarían y devolverían el resultado estimado del análisis”.
Castro calcula que a principios de 2017 ya podrán tener listo un primer producto en fase beta disponible para personas que quieran probarlo a través de plataformas de crowdfunding como Indiegogo. “Después, con la financiación adecuada, podríamos desarrollar un producto final que cumpla las regulaciones europeas a principios de 2019. Esto incluiría mejoras en el prototipo y validación clínica en una muestra significativa de pacientes para demostrar la capacidad de la tecnología”, concluye.
(SINC)