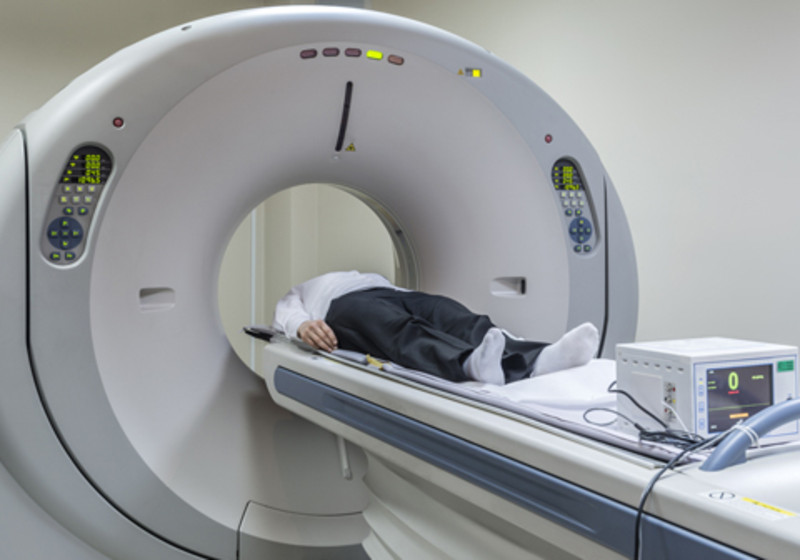
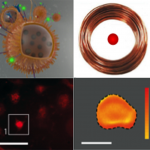
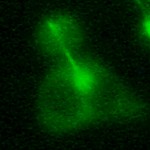
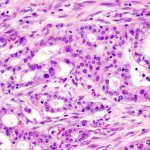
Allá por los años 90 del pasado siglo se descubrió que, bajo la acción de campos magnéticos alternos, las nanopartículas magnéticas absorbían gran cantidad de energía. De aquel hallazgo nació la hipertermia magnética, una terapia experimental contra el cáncer en la que partículas magnéticas estratégicamente colocadas en los tumores se convierten en fuente de calor.
Las nanopartículas emiten en forma de calor la energía que absorben del campo magnético alterno que se les aplica desde el exterior, provocando un aumento de temperatura en los tumores.
Según el físico Eneko Garai, de la Universidad del País Vasco, este sistema ofrece varias ventajas: «Por una parte, los campos magnéticos que se utilizan no son perjudiciales para el organismo, es decir, no producen calor, por lo que no afectan a las zonas sanas del cuerpo. Por otra, las nanopartículas pueden rodearse de ligandos. Por lo general, las partículas son de óxido de hierro, mientras que el ligando consiste en una capa elaborada con moléculas orgánicas. Gracias a este sistema, las nanopartículas pueden adherirse a las células tumorales, sin afectar a las células sanas».
Hay varios métodos para subir la temperatura, según los cuales se clasifican los tratamientos de hipertermia. En la hipertermia por radiofrecuencia, por ejemplo, se utilizan corrientes eléctricas inducidas por ondas electromagnéticas para aumentar la temperatura de los tumores, y antenas para concentrar en estos el calor.
La colocación de dichas antenas junto a los tumores se hace mediante cirugía. En la hipertermia por ultrasonidos, el calentamiento se efectúa mediante vibraciones; en la hipertermia por láser, en cambio, se excitan mediante un láser de infrarrojos las nanopartículas de oro o de plata que se colocan junto a los tumores para calentar las células tumorales.
Una técnica antigua con nuevas aplicaciones
Según Garaio, el resultado más relevante de su investigación es el siguiente: «Hemos fabricado un instrumento para medir la tasa específica de absorción de las nanopartículas; a continuación, hemos construido diversos modelos para calcular la tasa de absorción específica y para saber cómo cambian la forma, el material y los ligandos de las nanopartículas».
Por lo que a las pruebas de laboratorio se refiere, «hemos inducido una necrosis en los hígados de tres ratones, sin provocar daño alguno en las células sanas de dichos órganos», señala el investigador.
La eficacia del calor contra los tumores ya era conocida por los médicos hace más de mil años, y hace unos 200 se les provocaba fiebre a los enfermos, para que el calor combatiera los tumores. En eso consiste, resumidamente, la hipertermia», explica Garaio.
«Pero el calor no debe administrarse en cualquier zona del cuerpo, ni de cualquier manera: hay que aplicarlo solo a los tumores, a una temperatura que oscile entre los 41 y los 46 °C. Ese es el intervalo de temperatura en el que la hipertermia magnética es más eficaz», subraya el autor de la tesis.
Referencias bibliográficas
E Garaio, J M Collantes, F Plazaola, J A Garcia, I Castellanos-Rubio. ‘A multifrequency eletromagnetic applicator with an integrated AC magnetometer for magnetic hyperthermia experiments’, Measurement Science and Technology, 2014. Este artículo ha recibido recientemente el premio Outstanding Paper Award de la publicación Measurement Science and Technology.
H. Khurshid, J. Alonso, V. Sankar, Z. Nemati, M.H. Phan, H. Srikanth, E. Garayo, J.A. Garcia, ‘FeCo nanowires with enhanced heating powers and controllable dimensions for magnetic hyperthermia’, Journal of Applied Physics, 2015.
E. Garaio, O. Sandre, J. M. Collantes, J. A. Garcia, S. Mornet, and F. Plazaola, ‘Specific absorption rate dependence on temperature in magnetic field hyperthermia measured by dynamic hysteresis losses (AC Magnetometry)’, Nanotechnology, vol. 26, p. 015704.2015.
(UPV/EHU)