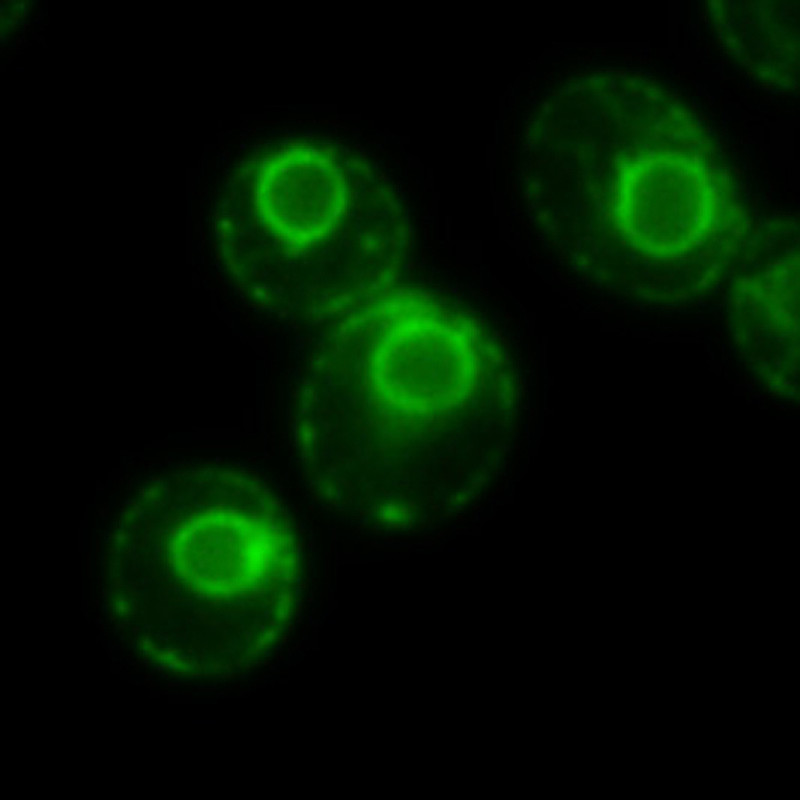
Un equipo de investigadores del IDIBAPS ha descubierto cuál es el mecanismo por el que dos orgánulos celulares, los cuerpos lipídicos (CL) y las mitocondrias, interaccionan para intercambiar los ácidos grasos que contienen los primeros para que las mitocondrias puedan producir energía cuando faltan los nutrientes. Esto se consigue gracias a unos microtúbulos especiales, como una especie de autopistas, sobre los que se colocan los CL y se desplazan hasta llegar a las mitocondrias.
El trabajo lo publica la revista Nature Communications y está liderado por Albert Pol, profesor ICREA del equipo Compartimientos intracelulares y señalización del IDIBAPS y profesor asociado de la Facultad de Medicina de la Universidad de Barcelona (UB), en colaboración con la Universidad de Queensland (Australia) y la Universidad de California (EE UU).
Las grasas son indispensables para la vida, pero muy tóxicas en exceso. En todas las células encontramos CL, unos orgánulos que almacenan el exceso de ácidos grasos que llega a la célula para reducir su toxicidad y poder suministrarlos cuando hay un requerimiento de energía.
Aunque su función está bien descrita en los adipocitos, las células del organismo especializadas en la acumulación de grasa, poco se sabe sobre la función de los CL en el resto de células y el mecanismo por el que interactúan con otros orgánulos celulares.
Para los expertos, conocer estos mecanismos sería de gran importancia dado que una acumulación excesiva de CL es la causa de enfermedades asociadas con la obesidad, como la diabetes tipo II, y de la aterosclerosis, como el síndrome metabólico o el hígado graso.
Los investigadores han visto que cuando se retiran los nutrientes de las células en cultivo, el patrón de distribución de los cuerpos lipídicos cambia y pasa de ser central, alrededor del núcleo, a periférico y disperso por el citoplasma.
Al profundizar sobre el mecanismo por el que esto sucede, han descubierto que intervienen un tipo especial de microtúbulos del citoesqueleto, el entramado tridimensional que organiza las estructuras internas de las células e interviene en el transporte y la división celular.
Los CL se disponen y se desplazan por sobre estos microtúbulos, al final de los que se encuentran las mitocondrias, facilitando que los ácidos grasos se puedan transformar en energía. Este mecanismo sirve para que la célula obtenga energía de una forma rápida y eficiente cuando faltan los nutrientes.
Conocer las causas
Otra de las novedades de este trabajo es que, para que todo esto suceda, se necesita la activación de una enzima conocida como AMPK (proteína quinasa activada por AMP), que es un sensor de energía celular que ayuda en el balance energético y el consumo de calorías.
Los investigadores han demostrado que la AMPK actúa de forma simultánea aumentando la movilidad de los CL, reorganizando la red de microtúbulos y activando a las mitocondrias, tanto en condiciones normales como en ayuno
Muchas enfermedades tienen su origen en una deficiencia en los mecanismos bioenergéticos de las células, y la acumulación de CL en diferentes tejidos está correlacionada con diferentes patologías de gran prevalencia.
Este artículo demuestra cuál es el mecanismo por el que se movilizan los CL para la producción de energía, tanto en condiciones en las que faltan los nutrientes como en condiciones normales.
Con este descubrimiento se podrá profundizar en el conocimiento de las causas y en el tratamiento de enfermedades como la diabetes o la aterosclerosis. «Con la administración de un fármaco como la metformina, uno de los más utilizados en el tratamiento de la diabetes de tipo II, se desencadenan todos los procesos que movilizan los CL, quemando las grasas y doblando la eficiencia en la producción de energía», concluye Albert Pol.
Referencia bibliográfica:
Albert Herms, Marta Bosch, Babu J.N. Reddy, Nicole L. Schieber, Alba Fajardo, Celia Rupérez, Andrea Fernández-Vidal, Charles Ferguson, Carles Rentero, Francesc Tebar, Carlos Enrich, Robert G. Parton, Steven P. Gross & Albert Pol. «AMPK Activation Promotes Lipid Droplet Dispersion on Detyrosinated Microtubules to Increase Mitochondrial Fatty Acid Oxidation». Nature Communications. DOI:10.1038/ncomms8176