Un equipo de la Universidad de Oviedo, dirigido por el catedrático de Bioquímica y Biología Molecular Carlos López-Otín, en colaboración con el Instituto Josep Carreras y las universidades de Barcelona y Harvard (EE UU), ha identificado un nuevo mecanismo molecular alterado durante el envejecimiento.
Este descubrimiento, publicado en la revista Nature Cell Biology, les ha permitido desarrollar un tratamiento que duplica la esperanza de vida de ratones con envejecimiento acelerado. El artículo, además, ha sido seleccionado para ocupar la portada del número de agosto de esta prestigiosa revista.
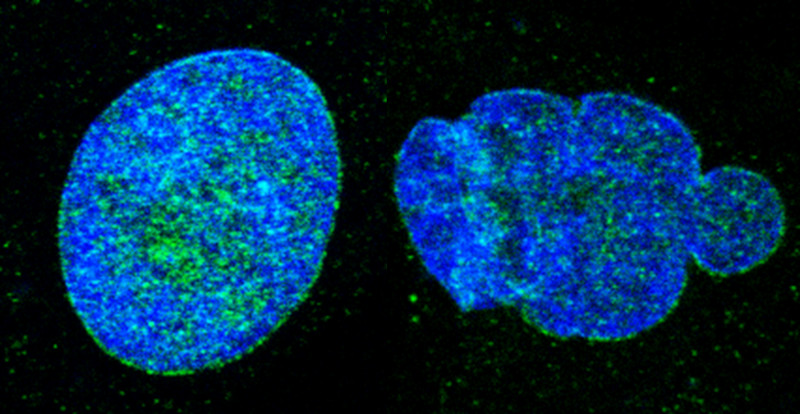
Los investigadores se centraron en el estudio del proceso de reprogramación celular, que facilita la transformación de células adultas en células madre inducidas (iPS), capaces de generar cualquier tipo celular del organismo. El proceso de reprogramación implica el rejuvenecimiento celular y requiere la eliminación de las alteraciones moleculares y celulares asociadas al envejecimiento.
Sin embargo, la reprogramación de células procedentes de pacientes con envejecimiento acelerado o de individuos de edad avanzada es muy ineficiente debido a las múltiples alteraciones acumuladas en sus células.
Por ello, el objetivo inicial de este trabajo consistió en identificar las alteraciones presentes en las células de pacientes con los síndromes progeroides de Néstor-Guillermo o Hutchinson-Gilford, que recapitulan fielmente muchas de las alteraciones asociadas al envejecimiento normal.
“El estudio de estas patologías presenta un gran interés biológico por las claves que pueden proporcionar acerca del envejecimiento normal y por la posibilidad de ensayar aproximaciones terapéuticas dirigidas a paliar o a retrasar sus efectos”, señala López-Otín.
Los expertos observaron que las células procedentes de estos pacientes o de individuos de edad avanzada presentaban una hiperactivación de procesos inflamatorios celulares. Sorprendentemente, “el tratamiento con fármacos antiinflamatorios aumentó la eficiencia de la reprogramación celular hasta niveles comparables a las células procedentes de individuos jóvenes”, resalta José María Pérez Freije, codirector del trabajo.
“Es la primera vez que se relaciona la hiperactivación de rutas bioquímicas de inflamación con los procesos de reprogramación celular”, apunta Fernando G. Osorio, otro de los autores de este estudio.
Aplicaciones clínicas
Con el fin de trasladar estos resultados hacia posibles aplicaciones clínicas, los investigadores identificaron un componente esencial de la respuesta inflamatoria implicada en este proceso, la proteína DOT1L. Esta proteína tiene la capacidad de regular numerosos genes implicados en el proceso de reprogramación celular y bloquea la formación de células madre iPS.
Tras administrar inhibidores de DOT1L a células humanas y ratones con envejecimiento acelerado, observaron una mejoría extraordinaria de todos los síntomas asociados al envejecimiento, así como un aumento de la esperanza de vida de estos ratones de más del 65%.
Estos resultados “superan ampliamente los obtenidos con las estrategias terapéuticas desarrolladas previamente para el tratamiento de los síndromes de envejecimiento acelerado sin presentar efectos secundarios aparentes”, comenta Clara Soria-Valles, primera firmante del trabajo.
Este descubrimiento tiene sus antecedentes en trabajos anteriores de este grupo publicados en Nature, Nature Medicine, Cell y Science Translational Medicine, en los que describieron diversos mecanismos implicados en el envejecimiento acelerado y el desarrollo de las primeras terapias para estos síndromes. Algunas de estas terapias se encuentran actualmente en ensayos clínicos para el tratamiento de pacientes con envejecimiento acelerado.
Puesto que los inhibidores de DOT1L están siendo empleados para el tratamiento de algunos tipos de leucemia, “es posible que se puedan ensayar en pacientes con progeria en un futuro próximo, solos o en combinación con otros agentes terapéuticos”, asegura Freije.
Este trabajo “demuestra la utilidad del estudio de los mecanismos implicados en la pérdida de plasticidad celular que acompaña al envejecimiento para identificar nuevas dianas terapéuticas que permitan intervenir sobre este proceso natural”, concluye López-Otín.
Referencia bibliográfica:
Clara Soria-Valles, Fernando G. Osorio, Ana Gutiérrez-Fernández, Alejandro De Los Ángeles, Clara Bueno, Pablo Menéndez, José I. Martín-Subero, George Q. Daley, José María P. Freije y Carlos López-Otín.
(UNIOVI)